文|氨基观察
创新药就像挖矿,临床数据是 “挖出来的是真正的矿”的证明,所有药企都是靠这个证据去融资、BD、申请药物上市。
因此,某种程度上,临床数据是药企最宝贵的财富。这也是为什么,生物科技行业极为重视知识产权保护,比如通过专利、著作权、商业秘密等方式对这些数据本身进行保护。
然而,专利能够保护的仅是很少一部分,大量的具体试验数据虽然不能申请专利,但对药品审批来说又至关重要。最直观的例子,莫过于仿制药的注册审批基于新药的试验数据,可以免于重新进行临床试验,从而大大节省时间和资金成本。
但对于原研药来说,经历“双十”考验获批上市后,若专利保护期已届满或即将届满,且没有额外的制度保护,那将意味着,其很难在有限的时间内收回成本,收益也就无从谈起。这会极大降低药企的创新、研发积极性。
倘若大量药企的创新回报不及预期,整个行业的投资生态也将遭受冲击。毕竟,投资最重要的是便是预期,没有人愿意投资于自己无法掌控/预期的东西。
从这个角度来说,创新药关键的知识产权不仅是专利,更包括药品试验数据保护(RDP)。因为,这可以防止竞争对手在一定时期内,利用自己的临床数据申报仿制药上市。
比如最早实行RDP制度的美国,其规定自生物创新药上市日起,12年内FDA不得批准仿制药的上市申请。其底层逻辑在于,谁做原始的安全性有效性数据,谁拥有数据的所有权,谁就应该得到相应的保护。
那么,药品试验数据保护到底是什么,为什么它比专利保护还要重要?
/ 01 / 拦截仿制药的利器
众所周知,新药研发是一个风险高、投资大、周期长的过程,药物有效性与安全性数据的获得需要进行长期推进和不断拓展的临床试验,并为此持续投入大量的人力与物力。
因此,如果对原研药企业付出巨大代价取得的药品试验数据不加以保护,这会削弱原研药企业的研发积极性,同时也会影响原研药企业的持续研发投入,最终影响药品的可及性。
药品试验数据保护制度起源于美国1984年通过的《药品价格竞争和专利期补偿法案》(《Hatch-Waxman法案》)。
这个法案首次明确提出了药品“数据保护”,确立了针对药品试验数据的独占保护制度。
FDA则在Hatch-Waxman法案之上,依据药品注册路径的不同给予了新化学实体(NCE)、全新的生物药实体(NBE)不同时长的保护周期。其中,NCE最长保护期为7.5年,NBE最长达12年,无论是NCE还是NBE,保护方式都为“不受理+不批准”,比如NBE上市4年内不受理仿制药上市申请,4年后可以受理申请,但8年内不得批准上市。
简单来说,所谓数据保护,就是监管机构在一定时间内不可以依赖原研公司提交的数据批准潜在的仿制药品进入市场,直接延迟仿制药进入市场的时间。
当然,在试验数据保护期结束后,FDA只需要审查仿制药是否与新药具有生物等效性即可。
为了保护本土药企,美国极力向其他国家推行该制度。作为国际协议,《与贸易有关的知识产权协议》(TRIPS协议)最早引入了药品试验数据保护制度,并成为了最早明确规定药品实验数据保护内容的国际标准。而后日本、欧盟等国家率先响应并积极实施,至今,全球已有多个国家以法律法规的形式对药品试验数据保护加以规制。
你可能会疑惑,药企已经享有专利保护,为什么还要数据保护?
那是因为,只有专利是不够的,知识产权保护需要贯穿创新药的全生命周期,尤其是对于生物药来说。
/ 02 / 额外的安全感
专利保护和数据保护,可以看做是两种具有互补作用的知识产权保护方式,都有助于激励开发创新药所需的巨大投资。后者则为药企提供了急需的额外安全感。
鉴于原研药的临床试验充满变数且耗时长久,当药物最终获批上市时,其法定专利保护期可能已经或即将结束。
在没有额外保护机制的情况下,其他企业可以选择开发、改良含有相同活性成分和相同适应症的同品种药品,并申请仿制药的注册。
对于前期投入成本巨大的原研药企来说,这种情况将不利于其收回成本并获得收益,进而可能降低原研药企的研发积极性。
由于各国专利规则的不同,对于某一新分子实体,临床实验可以证明其安全性,但往往一个专利文件会有各种各样的规定。特别是生物制剂相较于小分子药物,更难以通过专利手段抵御生物类似物的挑战。如果监管机构允许利用相同数据批准相似药物,那么专利法所能提供的保护力度将大打折扣。
除了生成相关数据的成本高昂,生物技术发明专利保护资格的不确定性以及有效执行这些权利的能力也进一步凸显了监管数据保护的必要性。
而数据保护则不同,药企做出来的全套数据都会得到保护,仿制药方做出来的数据也会得到保护。也就是说即使原研药享有数据保护,也不会妨碍仿制药独立进行全部临床试验,独立产生安全性有效性的临床数据。这是数据保护和专利保护不同的地方。
当然,对于药企来说,相比专利保护,数据保护最大的不同在于,其是在获得上市许可之后才开始起算,期限和效力均十分明确,能够有效阻止仿制药依赖原研药临床数据获得上市许可。
因此,从这个角度来说,RDP制度的重要目的之一,就是赋予原研药在上市后对其原始数据享有一定期限的市场独占期,通过不予批准其他企业利用未披露数据进行的仿制药或新药申请,为原研药企提供额外的保护。
/ 03 / 稳定回报预期
2009年7月,美国国会召开听证会,研究美国生物制剂的12年监管数据保护期的立法提案。第二年,《生物制剂价格竞争和创新法》签署成为法律,从美国监管机构首次批准之日起,新生物制剂的数据排他性为期12年。
可以说,除了自由定价,正是对于知识产权的全方位、严密保护,造就了美国生物科技行业的蓬勃与繁荣。
底层逻辑在于,这让大量VC/PE看到了未来回报的预期。
风投资金对于生物技术行业至关重要,而如果看不到未来的回报“承诺”,投资机构没有理由投资于这样一个高成本、高风险的行业。这种“承诺”,一方面取决于药企的研发实力,机构的投资能力,另一方面则有赖于制度保护。
知识产权保护,包括专利和数据保护,是创新药企的根基,也是投资的基础。没有人愿意投资自己无法掌控/预期的东西。
对于投资者来说,底线很简单:如果生物技术公司的临床数据在合理的时间内受到保护,它们更愿意加入这场赌局。
因为,它们往往根据随着时间的推移的回报率来证明其合理性。而获得的回报,则取决于投资的持久性——换句话说,创新药将产生多长时间的现金流和利润。
这种情况下,监管数据保护至关重要。因为正如前文所说,专利法在某种程度上为药企提供了这种保护,但并不完全。
而在一些投资人士看来,当前趋势还在发生变化,由于一些最高法院的其他裁决,专利法今天提供的保护更少。因此,在他们眼中,数据保护变得更加重要。
刨除美国诉讼的天文成本,对于初创公司,监管数据保护在实践中非常重要,因为你不能指望能够通过漫长的专利诉讼,来维护自己的权利。
简单来说,专利和RDP在内的产权保护,不仅让创新药企,也让行业的另一重要参与者——投资机构,对于创新药这门生意的投资回报,预期变得更加稳定。
/ 04 / 是否破坏了药物的获取?
当然,市场也担忧,RDP通过延长新药享有的市场排他性期限,会让药企变得更加垄断,进而影响药物的可及性,并会将医疗保健成本推高到不可持续的水平。
然而,日内瓦网络的研究表明,这种担忧或许是没有根据的。比如加拿大和日本子,它们近年来都延长了各自的RDP期限,但数据显示,在变化之前和之后的几年里,国家药品支出占GDP的百分比仍然几乎持平。
另外,有机构统计53个国家的市场数据后,的除了RDP反而能够增加创新药物的可及性。
2018-2022年,全球推出的所有创新药物中获批创新药物的比例,具有RDP的市场平均在全球至少一个市场拥有31.5%的创新药物,而没有RDP的市场平均有11.1%的创新药物可用。
这意味着,RDP市场中的患者可及的创新药物数量是没有RDP市场的患者的3倍左右。
造成这种差异的原因之一是,与其他知识产权保护机制一样,RDP加强了药企在一市场推出创新药物的立项依据。因为药企将有更好的机会享受一段保护期,在此期间它们可以产生收入,以收回开发和推出创新药物的成本。
此外,数据显示,在有RDP的市场上进行了更多的临床试验。比较在有和没有RDP的市场进行的平均临床试验数量,发现有RDP的市场平均每百万人有21项临床试验,而没有RDP的市场平均有4项。
这一数据也能够说明,RDP正向激励了创新药物临床研发。
而在业内人士看来,实施RDP也有可能会鼓励更多的“创新”。核心在于,数据保护提供了另一种形式的知识产权保护,会推迟生物仿制药公司将产品推向市场,除非它们自行取得的证明药品安全性、有效性的试验数据。
/ 05 / 国内何时跟上
如下图所示,全球拥有高度创新的生物制药行业的主要市场,基本拥有强大的知识产权保护和执法体系。美国对于创新生物制剂的数据保护期为最长达12年,欧盟采取“8+2+1”的保护模式,日本对创新药的保护期由6年延长至8年,加拿大则采用“6+2”的保护模式。
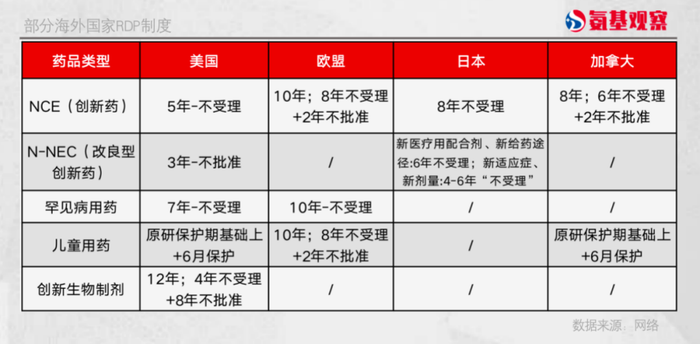
回到国内来说,随着创新药领域的大步发展,监管已经在最新的《专利法》修正案中加强了对创新药的知识产权保护。然而与国际水平相比,国内医药创新知识产权保护体系仍有待完善,数据保护具体条例还有待进一步落地。
事实上,早在本世纪初加入WTO后,我们国家便签署了TRIPs协议,并2002年实施的《药品管理法实施条例》中引入了相关数据保护内容。但截至目前,仍处于有总体规定、无实施细则的状态。
真正的改革、完善序幕应当是始于2018年,药监局出台《药品试验数据保护实施办法(暂行)(征求意见稿)》,系统性制定药品试验数据保护制度向社会公开征求意见;2022年5月,药监局综合司发布“公开征求《中华人民共和国药品管理法实施条例(修订草案征求意见稿)》意见”,将数据保护期统一设立为药品注册上市后6年。
同年7月,药监局在回复人大代表的相关提案中表示,待《药品管理法实施条例》修订实施后,将按照立法程序和要求,统筹安排《药品试验数据保护实施办法(暂行)》工作进展。
期待相关制度能够早日颁布实施,进一步完善我国医药行业的知识产权保护环境。



评论