文|动脉新医药
6月28日,北京绿竹生物技术股份有限公司(以下简称“绿竹生物”)在港交所提交了上市申请,这是一家研发人类疫苗、治疗性生物制剂的生物技术公司,主要聚焦于传染性疾病、癌症、自身免疫性疾病领域。
同一天,绿竹生物宣布完成了约2.18亿元的C轮融资,由华普海河生物医药基金、亦庄生物医药基金、信银振华等机构联合投资。这是绿竹生物今年内完成的第二笔、一年时间内完成的第三笔大额融资。
此前,绿竹生物分别在2021年8月和2022年1月完成了3.5亿元B轮融资和1.2亿元B+轮融资,2019年至今,绿竹生物四轮融资总计9.38亿元。接连获得了轩弘基金、銘丰资本、陕西金控/新时代资本、铭盛资本以及建银国际和两家A+H上市公司泰格医药、丽珠医药的投资认可。
绿竹生物成立于2001年11月,公司创始人均来自北京生物制品研究所,由前北京生物制品研究所研究员孔健、副研究员蒋先敏和张琰平联合创立。
针对当时国内外无可用于2岁以内儿童预防流行性脑脊髓膜炎感染的疫苗的现实,结合已掌握的多糖蛋白质偶联技术,绿竹生物成功开发出了多种细菌多糖蛋白结合疫苗和高纯度低热原的多糖疫苗(均已转让给上市公司智飞生物),成为全球首家开发出A群C群脑膜炎球菌多糖结合疫苗的企业。

经过二十余年的发展,绿竹生物依然深耕于疫苗及治疗性生物制剂赛道,并且已经搭建了创新的精准蛋白工程平台,助力公司开发包括候选人类疫苗、单克隆抗体、双特异性抗体等药物形式在内的在研产品。
01 LZ901有望成为首款国产带状疱疹疫苗
目前,绿竹生物旗下在研管线包括3款处于临床研究阶段的产品,和4款处于临床前研究阶段的候选药物。

绿竹生物的3款临床在研产品分别是:候选疫苗LZ901、候选抗体注射产品K3和K193。其中,候选疫苗LZ901和候选抗体注射产品K193是公司具有自主知识产品的创新药;而抗体注射产品K3则是公司基于阿达木单抗研发的生物类似药。
LZ901:中国首款也是唯一一款寻求全球申报的带状疱疹疫苗
LZ901是具有四聚体分子结构的带状疱疹疫苗,用于预防50岁及以上成人水痘带状疱疹病毒(VZV)引起的带状疱疹。该疫苗由在CHO细胞上表达的VZV gE与ⅠgG的两个Fc片段构成,与自然发生的VZV gE相比,LZ901能表现出更好的免疫原性,诱导出更高水平的中和抗体滴度。
根据已有的临床前研究数据显示,LZ901有着优异的免疫原性、有效性和安全性,同时可以诱导强烈的特异性体液和细胞免疫。
目前,绿竹生物已在中国完成LZ901的Ⅰ期临床试验,目前正进行Ⅱ期临床试验。公司预计于2022年第四季度在中国完成LZ901的Ⅱ期临床试验,于2023年第一季度启动Ⅲ期临床试验,并于2024年第二季度向国家药监局提交LZ901的NDA。
同时,公司也已于2022年1月向FDA提交LZ901的IND申请,并计划于2023年在美国启动Ⅰ/Ⅱ期临床试验。
由于更容易感染带状疱疹的老龄化人口不断增长,带状疱疹在中国的发病率越来越高。根据弗若斯特沙利文的资料,中国50岁及以上人群的带状疱疹新病例从2015年的250万例增加到2021年的390万例,复合年增长率为7.8%,预计2025年将增加到490万例;2021年至2025年的复合年增长率为6%,到2030年将进一步增加到600万例,2025年至2030年的复合年增长率为4.2%。
随着公众对带状疱疹的认识不断提高,以及可用的带状疱疹疫苗产品数量增加,中国的带状疱疹疫苗市场有望显著扩大。
根据弗若斯特沙利文资料,按销售收入计,中国带状疱疹疫苗市场从2015年的零增加至2021年的人民币6亿元,并预计将增加至2025年的人民币108亿元,2021年至2025年的复合年增长率为103.8%,以及将进一步增加至2030年的人民币281亿元,2025年至2030年的复合年增长率为21.1%。
但是中国市场仅有一款获批的带状疱疹疫苗,即葛兰素史克的Shingrix 。因此,LZ90难免会被拿来和葛兰素史克的Shingrix 进行对比。
在招股书中,绿竹生物指出,LZ901与目前已经在中国上市的带状疱疹疫苗相比,具备多个优势:不仅价格低廉、副作用小;而且分子结构具有优势,高度稳定、易于储存和运输,使用方便;还具有强大的保护作用。
具体而言,LZ901的零售定价预计约为500元至800元/针,每个疗程共注射两针,和Shingrix 定价约1600元一针,每个疗程共注射两针相比,价格优势明显。
在BALB/c小鼠的研究中,绿竹生物的LZ901能够诱导更强烈的细胞免疫反应,更高地表达多种类型的免疫细胞启动生物标志物。
在副作用控制方面,由于LZ901液体制剂只含有氢氧化铝佐剂,且不含免疫刺激物,降低了注射部位出现严重不良反应的可能性。同时,因为LZ901采用高稳定性液体配方,更易于储存和运输,使用方便。能在37℃时稳定存储两周,在25℃时稳定存储12周,在2-8℃时稳定24个月。
K3:针对自身免疫性疾病,即将进入临床Ⅲ期
K3是重组人抗TNF-α单克隆抗体注射液,属于阿达木单抗的生物类似药,主要用于治疗各种自身免疫性疾病,如类风湿性关节炎、强直性脊柱炎和斑块状银屑病。
阿达木单抗是一款的TNF-α抑制剂,由艾伯维以品牌名称Humira 销售。Humira 于2010年获得NMPA批准,并纳入国家医保药品目录,其平均售价于2015年最初为每盒7729元,并由2019年的5572元降至2020年的1258元,与2019年相比,2020年Humira 的收入直接贡献440%的增幅。
由于阿达木单抗适应症范围广、市场需求量大以及新型生物类似药产品不断出现,阿达木单抗在中国的市场规模正快速增长。按销售收入计,阿达木单抗在中国的市场从2015年的2亿元增至2021年的16亿元,复合年增长率为41.3%,并预计从2021年至2025年按42.7%的复合年增长率增至2025年的68亿元。
根据弗若斯特沙利文的资料,目前总计有6款阿达木单抗的生物类似药在中国获批,分别是Qletli 、Sulinno 、安建宁、汉达远、泰博维和君迈康,以及10款正在中国开发的阿达木单抗生物类似药。
绿竹生物以阿达木单抗的抗体结构为基础开发了K3,使该抗体在人体中使用时的安全性最大化。K3的药代动力学、安全性和免疫原性评估表明,它与阿达木单抗高度相似,K3与阿达木单抗之间没有临床意义上的差异,表明K3在治疗类风湿性关节炎、强直性脊柱炎和斑块状银屑病等自身免疫性疾病方面的潜力。
目前,绿竹生物已经在中国完成了K3治疗多种自身免疫性疾病的Ⅰ期临床试验。根据绿竹生物招股书披露,国家药监局审评中心“确认绿竹生物K3的中国Ⅰ期临床试验经完成,且不反对直接进行Ⅲ期临床试验。”所以,绿竹生物的K3在中国将跳过Ⅱ期试验,直接进入Ⅲ期临床,公司计划于2023年第二季度在中国启动该Ⅲ期临床试验。并规划于2024年第二季度完成Ⅲ期临床试验,同年第四季度向国家药监局提交BLA。最终预计K3于2025年获得国家药监局的BLA批准。
在定价方面,K3预期按每剂约400元至500元的零售价定价。
K193:全球首款不对称结构CD19/CD3双特异性抗体
K193是全球首款具有不对称结构的CD19/CD3双特异性抗体,用于治疗B细胞白血病和淋巴瘤。K193能够与人类B细胞表面的CD19和T细胞表面的CD3结合,从而启动T细胞杀死与白血病和淋巴瘤相关的B细胞和B细胞来源肿瘤细胞。
K193在临床前研究中显示出很高的体内外抗肿瘤活性,其启动T细胞杀死与白血病和淋巴瘤有关的B细胞和B细胞来源肿瘤细胞的能力比CAR-T疗法中常用的OKT3单克隆抗体高出10000倍。
目前,绿竹生物正在中国进行K193的Ⅰ期临床试验,并预计于2022年第四季度完成Ⅰ期临床试验。长远来看,2027年第四季度公司在中国完成K193的Ⅱ期临床试验,并于2027年向国家药监局提交NDA。
据悉,中国只有一个双特异性抗体注射液(CD19-CD3)获批,即安进的Blincyto 。根据弗若斯特沙利文的资料,除了K193,中国还有两款已在国家药监局药物评估中心(CDE)注册的双特异性抗体注射液(CD19-CD3)正处于临床开发阶段,即健能隆医药技术(上海)有限公司的A-319和同润生物医疗的CN201。
与全球上市的治疗B细胞白血病和淋巴瘤的抗体注射剂相比,K193具有价格低廉、给药方便简单、亲和力强、副作用低的优势。据悉,K193零售定价预计为一个疗程约20万元,终身疗程另加20万元,总费用为人民币40万元;与Blincyto 一个疗程约36万元的零售价和Blincyto 一年约人民币150万元的治疗费相比,价格更实惠。
除了绿竹生物这3款已经进入临床研究阶段的在研产品,公司另有4款临床前研究阶段的管线分别是:重组水痘疫苗、重组狂犬病疫苗、治疗白血病的抗体注射产品K333及治疗淋巴瘤的K1932。
02 2021年研发投入超4000万,搭建五大技术平台
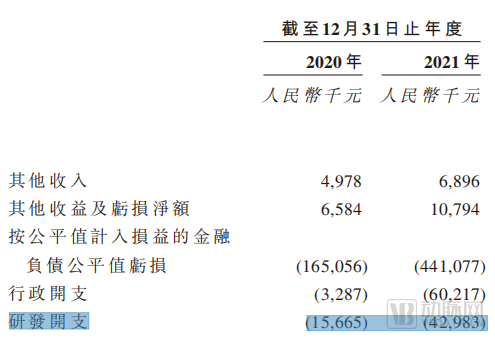
根据绿竹生物招股书数据,公司在2020年和2021年的研发投入分别为1566.5万元和4298.3万元,增加的研发支出主要因为公司第三方承包成本的提高。随着公司临床管线的推进,未来绿竹生物的研发投入也将会逐年提高。
在技术方面,绿竹生物的重组病毒疫苗,是基于抗原呈递技术和提高目标抗原的免疫原性的理念开发,在提高免疫原性的同时保留了天然抗原的主要结构。基于该技术理念,绿竹生物内部也开发了五个技术平台,分别是:
Fabite 技术平台:Fabite 是绿竹生物拥有知识产权的新一代双特异性抗体开发技术平台,可用于各种基于启动T细胞杀死癌细胞的免疫疗法。Fabite 优化了双特异性抗体的纯化过程,使单体达到高纯度。同时,绿竹生物开发了多种液体配方的双特异性抗体溶液,在2-8 C的储存条件下可稳定三年以上。
靶向重组抗原呈递技术平台:绿竹生物的靶向重组抗原呈递技术平台形成表达抗原的重组免疫复合物(RIC),并直接将病毒膜抗原呈递给APC。这一技术平台的技术极大地提高了抗原的利用效率,可以诱导出高滴度的特异性抗体和细胞免疫。此外,绿竹生物的靶向重组抗原呈递技术平台所表达的抗原含有多个片段可结晶(Fc)区域,这是对只表达单一Fc区抗原的传统融合蛋白技术的改进。
多糖-蛋白共轭技术平台:绿竹生物的多糖-蛋白共轭技术平台将细菌多糖与载体蛋白连接起来。这一技术平台可用于开发结合疫苗和抗体-药物偶联物。绿竹生物利用绿竹生物的多糖-蛋白共轭技术平台开发了三种细菌多糖-蛋白共轭疫苗,这些疫苗具有更强的免疫原性和稳定性,并且是易于施用的液体剂型。
蛋白纯化技术平台:绿竹生物开发了复杂重组蛋白的纯化技术,如人源化单克隆抗体和复杂糖基化蛋白。绿竹生物使用高速离心或深层过滤工作流程来分离细胞培养基中的蛋白,这在从可溶性蛋白质中去除细胞和细胞碎片方面非常有效。此外,绿竹生物在蛋白纯化过程中采用了一系列色谱技术,进一步提高纯度。作为最后的精纯步骤,绿竹生物采用尺寸排除色谱法,从而获得高纯度的相关蛋白。
蛋白稳定性技术平台:绿竹生物开发了多种高度稳定的人源性单克隆抗体、双特异性抗体和重组蛋白疫苗的液体制剂。它们能在溶液中保持大多数单克隆抗体或双特异性抗体的活性长达五年。同时,绿竹生物提供具有不同稳定机制的多种配方,以满足不同的抗体或抗原要求。绿竹生物的配方不含蛋白质,能够满足人类药物或特定检测系统的背景要求,并在免疫检测中,可以起到稳定酶及对照材料的作用。
哺乳动物表达技术平台:绿竹生物于2012年引入了Lonza的GSXceedTM表达系统。该系统涵盖了广泛的技术及工艺,如宿主细胞、表达载体和优化培养基,并为各种生物药物提供高质量、高效率及高容量的生产服务。




评论