文|氨基财经
国内内卷,导致PD-1千亿市场“消失”,创新药企们开始把目光放向海外。
一时间,PD-1出海潮汹涌。
2021年,仅K药、O药两大王牌产品全球销售额达到247亿美金。国产PD-1随便啃下一块骨头,都比在国内卷着要好。短期内无法被证伪的出海故事,也成为支撑投资者预期的关键。
不过,目前看起来,依靠性价比优势,在海外PD-1市场撕开一道口子的故事,似乎越来越不好讲。
近日,诺华在二季报中透露,将放弃申请与百济神州合作的PD-1单药针对非小细胞肺癌的上市申请。
这已经不是国产PD-1第一次出海遇阻了。近半年来,从信达生物、君实生物再到百济神州,多多少少都在PD-1出海方面遇到了挫折。
市场开始意识到,尽管国产PD-1有性价比优势,但在FDA审核趋严,产品临床进度和适应症开发都不占优势的情况下,翻越K药这座大山并不容易。
国产PD-1跨过大洋,在海外寻找第二增长曲线的梦,还能实现吗?
PD-1出海接连受阻背后
曾几何时,出海去寻找PD-1另一个可能的未来,是众多国产PD-1/PD-L1共同的希望。
但现实却很“残酷”,在信达生物PD-1出海被拒,君实生物、百济神州PD-1出海申请被延期后,又一个噩耗传来。
近日,诺华在二季报中披露,在与FDA沟通后,将不会再申报与百济神州合作的PD-1替雷利珠单抗单药治疗非小细胞肺癌的适应症。
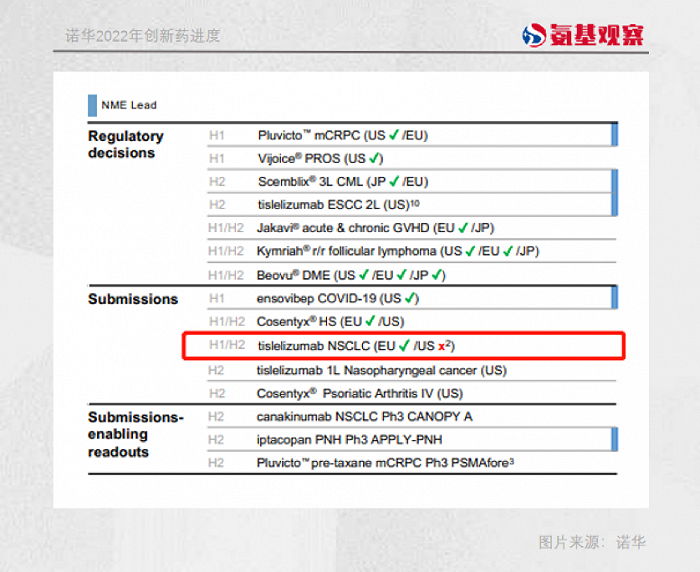
我们都知道,信达生物PD-1遭拒,是因为临床试验存在仅使用国内临床数据、采用无进展生存期而非总生存期为终点等瑕疵。
但是,百济神州的替雷利珠单抗对于非小细胞肺癌患者的临床,则是进行了全球多中心临床试验,并且是以总生存期为终点,那么,为什么还会出现问题?
对此,诺华首席执行官在电话会议中给出了答案。在和FDA沟通后,FDA认为百济神州对于非小细胞肺癌患者的Rationale-303研究,在患者人数方面和用药标准方面不能充分反映美国的情况。
具体来看,虽然Rationale-303为国际多中心临床试验,但在这项试验中肺鳞癌患者中亚洲人占比80.8%、白种人占比16.7%、其他人种占比2.4%,鳞癌患者中亚洲人占比77.4%、白种人占比18.5%、其他人种占比4%。
总体来看,入组亚洲人种比例较大。看起来,在FDA眼中,只做临床多中心实验是不够的,还需要考虑美国患者入组人数比例。
不过,虽然只是临床入组方面的原因,但诺华似乎已经对这一适应症单药疗法的未来不抱希望。毕竟,诺华在财报中的表述是“放弃”申报。这又是为什么呢?
某种程度上,是诺华意识到替雷利珠临床推进速度不占优势。毕竟,目前在美国,K药、O药都已成为非小细胞肺癌一线疗法的标准疗法。在这样的背景下,再推进单药二线疗法的意义相对不大。
固然,在非小细胞癌领域,替雷利珠还有希望,其联合TIGIT单抗头对头K药的临床依然在推进。不过,距离成功还需一定时日。短期内,诺华选择将希望放在其它适应症上。
从国内卷到国外,从大适应症卷到小适应症
国产PD-1扎堆出海,内卷已经从国内蔓延至国外,从大适应症蔓延至小适应症。
在非小细胞癌二线疗法遇阻后,诺华把目光瞄向了食管癌和鼻咽癌等。其中,鼻咽癌这一适应症被提上了日程,下半年将向FDA递交PD-1一线鼻咽癌上市申请。
实际上,诺华的做法并不令人意外。按照FDA此前对信达生物的要求,新PD-1要想在美国上市,就需要和现有标准疗法一较高下。而在美国,K药获批了几十个适应症,基本所有大适应症都能看到K药的身影。
这也就意味着,后来者想拿下大适应症避免不了和K药等先驱进行头对头临床试验。然而,头对头对比的代价极其高昂,一旦失败不仅意味着巨额临床费用打水漂,更意味着彻底失去翻盘希望。
因而,出海的国内药企选择避开K药的锋芒。在这种情况下,一些没有被K药踏足的小适应症成了香饽饽。
比如说诺华选择的鼻咽癌。鼻咽癌在亚洲人群中高发,但在美国属于罕见癌种,美国每年鼻咽癌患者不到2万人。目前,在美国尚无PD-1获批用于治疗鼻咽癌。
这也说明,鼻咽癌这一适应症在美国存在未被满足的临床需求。而对于这一适应症申报上市,FDA的监管或许会放松要求,更重要的是,无需与K药进行头对头临床试验。
所以,后来者选择鼻咽癌成功获批的几率,相比其他大适应症要大得多。也正因此,除了百济神州,国内不少出海玩家都不约而同地瞄准了这一适应症。
君实生物是最早向FDA提交PD-1单抗三线治疗鼻咽癌上市申请的药企,不过由于疫情原因,FDA对于特瑞普利单抗的审批被推后。去年,康方生物/正大天晴的PD-1也向FDA提交了三线鼻咽癌的上市申请。
如今,加上百济神州,一个小适应症仅国内玩家就有三家入局,竞争不可谓不激烈。
虽然小适应症是PD-1后来者逆袭的最佳途径,但随着PD-1竞争日益激烈,小适应症在美国上市的路也将越来越难。因为,按照FDA的要求,后来者都要展现出现优于现有疗法的实力才能够获批。
这也就意味着,即便在小适应症上,也是一场竞速淘汰赛。谁的申报速度快,谁就能率先上岸,否则可能连小适应症都上不了岸。
原本,国产PD-1出海的初衷是想改变内卷的命运,但没想到,最终还是逃不开内卷的命运。
出海的理想与现实
与国内一样,海外市场或许也会让不少PD-1玩家失望。
想当初,市场关于PD-1的未来大胆地做出了千亿市场的预测,但随着国产PD-1相继上市,一场场价格战先后展开,PD-1千亿市场化为泡影。
在这一背景下,国内药企纷纷瞄准海外。逻辑是,具有性价比优势的国产PD-1将会成为海外市场“鲶鱼”,拿下一定的市场份额。
大家都知道,美国是全球药价最高的地方,没有之一。在肿瘤治疗领域,美国随便一款肿瘤药物年治疗费用,超过10万美金是家常便饭。
PD-1抑制剂也是如此。国内PD-1年用药费用最低已经降至不到4万元,但K药在海外的年用药费用超过60万元。
很显然,在不缺支付能力的海外市场,药企拥有较大的定价权。针对这一情况,甚至诞生了专门引进me too类创新药的“价格屠夫”EQRx。
实际上,大投行们对于这门生意也较为看好。去年,摩根士丹利的分析师Matthew Harrison算了一笔账,替雷利珠单抗如果顺利获批,每年可能为诺华带来至少20亿美元的营收。
但如今看起来,在K药、O药占据绝对身位的海外市场,同质化产品似乎并不容易走上台来。即便后来者能通过差异化适应症打开美国大门,但在内卷之下,美国留给中国玩家本就不大的市场,又有多少利润可图呢?
历史总是惊人的相似。如今看起来,曾经PD-1千亿市场消失的故事,或许会在海外市场再次上演。而PD-1的今天,未必不会成为国内其他创新药的明天。
虽然国内创新药近年来蓬勃发展,但我们不得不承认的事实是,大部分的fast follow产品只适用于国内,放到海外市场上或许只能沦为slow follow。
换言之,海外市场要比国内更加残酷。虽然海外没有集采,但那里也并非舒适的避风港,而是另一个历练场。这也给国内创新药企提了一个醒,不论去到哪里,实力永远都是最好的通行证。



评论