文|氨基观察
一直以来,客观缓解率(ORR)都是抗肿瘤药物的临床替代终点之一。
客观缓解指的是“肿瘤病灶直径之和比基线水平减少相当高的水平”。通常情况下恶性肿瘤不经治疗不会自动缩小。客观缓解率越高,说明患者对治疗有积极响应。
国内外不少肿瘤药物,正是凭借着极高的客观缓解率,拿到了率先上市的门票。
不过,客观缓解率虽然能在一定程度上反映药物效果,但评价药效的金标准依然是总生存期(OS)。
而客观缓解率数据,与总生存期获益情况并不完全对等。
PI3K抑制剂就是一个最好的案例。曾几何时,凭借着客观缓解率的炸裂数据,一款款PI3K抑制剂获得FDA加速批准上市。
但遗憾的是,部分PI3K抑制剂并不能延长患者的生存期。
9月23日,FDA召开的肿瘤药物咨询会,便因此以压倒性的投票数据,反对PI3K抑制剂Duvelisib用于复发或难治性慢性淋巴细胞白血病(CLL)或小淋巴细胞淋巴瘤(SLL)。
事实上,今年以来FDA对于PI3K抑制剂的态度不断缩紧。先是对PI3K抑制剂凭借单臂临床上市的做法说不,后又对已经上市PI3K抑制剂的适应症价值给予否定。
一叶落而知秋,一个PI3K靶点遭退货背后,反映的则是客观缓解率与总生存期之间的矛盾。
如果抛开总生存期,只凭客观缓解率谈药物的抗肿瘤效果,不一定完全靠谱。
01 三十年背景的成熟靶点,展现惊人客观缓解率
PI3K抑制剂在今年水逆或许出乎所有人意料。
要说PI3K(磷脂酰肌醇3-激酶)是肿瘤治疗领域的成熟靶点,绝对没有人会有异议。毕竟,PI3K的发现已经有几十年,早在1988年科学家们就发现了PI3K信号通路。
在进一步的研究中,科学家们发现PI3K-AKT-mTOR信号通路能够控制多个细胞过程,包括代谢、运动、增殖、生长和存活,但其异常激活也会为癌细胞提供便利,是人类癌症中最常见的致癌事件之一。
对于PI3K所调控信号通路的机制已经很清晰。因而切断这一信号通路来控制癌症发生,也成为了理想的癌症治疗靶点。
事后来看,PI3K抑制剂成药性也被充分验证。目前为止,全球已经有5款PI3K抑制剂获批上市。根据这些获批产批公布的结果,客观缓解率数据都惊为天人。
2014年,吉利德的PI3K抑制剂idelalisib与安慰剂分别联合美罗华,治疗复发慢性淋巴细胞白血病(R-CLL)三期临床结果出炉:
Idelalisib组的ORR(客观缓解率)为81%,安慰剂组仅为13%,这意味着十个患者中八个都能出现肿瘤缩小,而在安慰剂组仅有一名患者出现反应。
基于这一优异的表现idelalisib率先上市,成为全球首个PI3K抑制剂。
如下图所示,另外几款PI3K抑制剂,在客观缓解率和无进展生存期上的表现也堪称亮眼。Duvelisib获批上市的适应症中,客观缓解率也是高达78%。
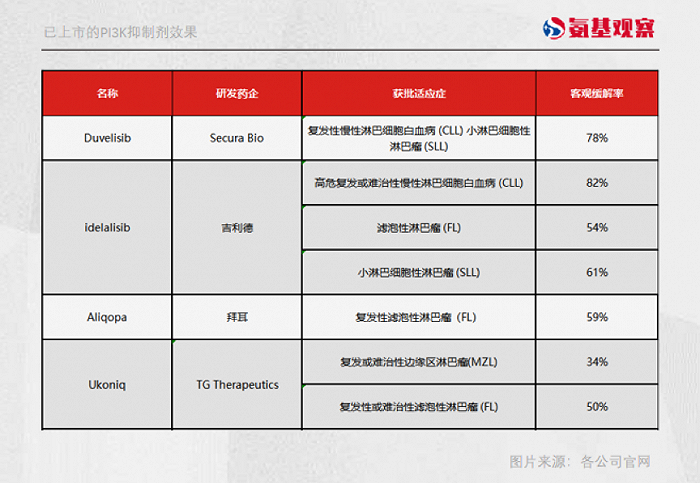
所以,彼时FDA凭借这些数据批准它们上市也无可厚非。
PI3K抑制剂也因此吸引了不少国内玩家入局。进度最快的是石药集团,今年3月其引进的PI3K抑制剂已经获批上市,正是Duvelisib这款产品。
此外,恒瑞医药、信达生物、君实生物等国内实力玩家的PI3K抑制剂也都在赶来的路上。如此多大药企,都在投入这一靶点的药物研发,从侧面也体现出了PI3K抑制剂的吸引力。
然而,即便是机制清晰、成药性被证实、大药企背书层层光环的加持下,PI3K抑制剂还是翻车了。
02 没能延长OS,“上岸”靶点也翻车
PI3K抑制剂最近一次的翻车记录,就发生在三天前。
9月23日,FDA召开了肿瘤药物咨询会,目的是针对已经获批上市的PI3K抑制剂Duvelisib三线治疗慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)适应症的去留做出抉择。
那么,一款已经获批上市的药物,为什么还会再次受到FDA的审判呢?
这是因为,此前这款药物获批是基于临床替代终点PFS与ORR做出的加速审批。
所谓加速批准,是FDA提供给那些用于治疗严重疾病新药的一条快捷通道,使得这些新药能依靠临床替代终点申报上市。
不过,此后这些药物还需要继续临床以证明药效,如果OS数据不及预期,那么仍然会被撤回适应症。如今,Duvelisib就遭遇OS数据不佳的困境。
在名为DUO的临床试验中,使用Duvelisib治疗的患者中位生存期为52.3个月,使用Ofatumumab治疗的患者中位生存期为63.3个月。
治疗组生存获益情况还不如对照组,这显然有点拉垮。
看到这里,你或许会感到疑惑,为什么PI3K抑制剂客观缓解率超高,却没能延长患者生存期呢?
答案或许是,火力太猛。
由于PI3K在细胞中广泛存在,要想达到抑制肿瘤的效果,就需要加大药物剂量。但与此同时,大剂量地对PI3K一刀切,势必会影响到其他细胞的正常作用,带来严重的副作用。
可以看到,Duvelisib组不良事件发生率高达15%,而Ofatumumab仅为3%。也就是说,Duvelisib对抗肿瘤用的是杀敌一百自损三千的招数,肿瘤消失了患者的身体也垮了。
显然,这并非一款优秀抗肿瘤药物所具备的特点,也是如此,FDA肿瘤药物咨询委员会的投票结果,以压倒性的数据反对Duvelisib获批的适应症继续上市。
03 肿瘤药物好与不好的评判标准,离不开“金标准”
PI3K抑制剂翻车也告诉我们,临床替代终点虽好,但不是值得我们百分百信任的标准。
种种事实证明,这些临床替代终点和总生存期之间,并不能完全画等号。
拿常用的临床替代终点ORR来说,它能够反映肿瘤病灶直径之和比基线水平减少的程度,是实体瘤疗效评价标准中的关键指标。所以客观缓解率的提高,也的确能说明患者对治疗有积极响应。
不过,ORR与OS的关系却并不是那么相关。虽然一些肿瘤药物前期能让ORR升高,但如果后续出现耐药肿瘤可能进展更快,并不会给OS带来提升。
此外,副作用对于肿瘤患者生存期的影响,也无法通过ORR体现。PI3K抑制剂使用临床替代终点翻车的案例,就是最好的例子。
事实上,因使用临床替代终点而翻车的例子,不仅限于PI3K抑制。
2021年FDA撤回的7个经加速批准上市的药物适应症,不少都是因为前期ORR数据可观,但后期的总生存期上没有展现优势。
比如说,K药此前被加速批准用于小细胞肺癌的三线治疗,依据就是客观缓解率。
但是2021年3月,因为在后续临床试验中,晚期SCLC患者一线使用K药+EP方案和安慰剂+EP方案的疗效显示,K药组的OS未达到统计学意义,这一适应症被撤回。
当然,在PD-(L)1的治疗过程中,也有些特殊情况是:呈现显著的总生存期获益,但是在ORR指标上却没有很大的效果。所以,ORR并不能准确地反映OS的变化情况。
不管怎么说,或许临床替代终点能够帮助药物率先上市,但如果没有OS数据做依托也难以走到最后。
正如统计学家Stephen Senn所说:
“替代终点和真实终点的关系就像支票和现金,你可以提前拿到支票,但也有可能会遭遇退票。”



评论