文|氨基观察
生物科技,是未来亦是未知。
创新,则有着矛盾而迷人的两面性,不到最后一刻,永远不能对一款药物下结论。
即便是一款看上去已经希望不大的药物,经过药物研发人员的妙手,也有可能再逢春。CTLA-4抑制剂便是典型。
作为全球首个问世的免疫检查点抑制剂,CTLA-4抑制剂问世即高点。由于严重的安全问题及单药疗效的局限,再加上后来者PD-1抑制剂的超强表现,CTLA-4抑制剂陷入低谷。
不过,研发人员从未放弃CTLA-4这一靶点。难产18年后,第二款CTLA-4抑制剂终于上市;不久前,BioNTech以高达2亿美元的首付款,与昂科免疫就CTLA-4抑制剂ONC-392达成合作。二代CTLA-4抑制剂开始走向舞台。
CTLA-4抑制剂的浮沉,只是创新药研发徘徊于生死线上的一个缩影。将创新的科研/技术发现转化成产业,转化过程充满不确定,有的迅速成功,有的黯然退场,更有的蹉跎百年。
在“下一个PD-1”的驱使下,IDO抑制剂高开低走,大药厂纷纷押注,却在5年间从倍受追捧,走到临床失败无人问津的地步;潜力十足的LAG-3抑制剂,成药性反复被质疑,历经30年才得以通过联合疗法问世;TIGIT靶点从明日之星再到多次临床失利暴击,阴霾重重,前后也不过三四年光景……
不止是免疫疗法与癌症,当下如日中天的生物导弹ADC,穿越百年才走进现实,历经三代药物更迭才见曙光;阿尔兹海默症,近20年无数药企前赴后继,砸下一个数千亿美金“天坑”后,Aβ单抗的前景仍有待观察。
开创性的研究往往如技术触发点一样,导致科学研究的爆炸式增长,但死神之于创新药本就如影随形。或许,也唯有抱着向死而生的信念,才能在创新药研发的竞技场杀出一条血路。
/ 01 / CTLA-4的高光与低谷
任何领域,第一名往往容易被人熟知,并在历史长河中留下深深印记。免疫疗法的发展则是例外,第二名PD-1有着远超第一名CTLA-4的声名。
在免疫检查点的发展历程中,第 个被确定的是细胞毒性T淋巴细胞抗原4(CTLA-4)。1996年,Leach、Krummel和Allison发现,小鼠的CTLA-4抗体可以诱导移植物的免疫排斥反应。
随后,关于这个靶点研究开始展开。1999年靶向CTLA-4的伊匹木单抗(Yervoy)诞生,在临床研究的推进下患者获益逐渐明确;2011年3月25日,Yervoy(Y药)在美国获批上市,成为全球首款免疫检查点抑制剂。
这是CTLA-4靶点的高光时刻。但头顶首款免疫疗法的光环,却没能让Y药得意多久。
上市初期,Y药对于黑色素瘤的治疗疗效突出,能够有效延长患者的生存期,但与此同时,Y药也出现了极高的副作用。数据统计表明,Y药引起的免疫相关不良事件出现在多达60%的患者中,其中10-30%被评定为极其严重的症状。
这是由于,CTLA-4本身具有正常的生理功能,缺乏CTLA-4会导致人体出现严重免疫相关不良事件。而Y药则会将细胞表面的CTLA-4带到溶酶体中降解,导致人体CTLA-4缺乏,由此导致严重免疫治疗相关不良反应。
在安全性桎梏下,CTLA-4抑制剂虽然抗肿瘤作用显著,但是用药安全窗口极窄,很难通过单药发挥效果。这也使得,CTLA-4抑制剂对抗肿瘤的真实实力一直被压制。
随着PD-1的问世,Y药的光环进一步淡去。
2014年,PD-1抑制剂K药、O药相继问世。与CTLA-4抑制剂相比,PD-1抑制剂有着更好的安全性,更强的效果。两相对比之下,CTLA-4曾经的拥趸者纷纷转战PD-1。
截至目前,FDA已经批准5款PD-1抑制剂上市,而获批上市的CTLA-4抑制剂仅有2款,第二款抑制剂的获批还是在2022年。
在销售额上,PD-1更是与CTLA-4拉开了巨大差距。2022年,PD-1抑制剂之王K药的销售额超过209亿美元,而同期Y药的销售额不过21.31亿美元。
不过,作为前辈的CTLA-4抑制剂也具有强劲的韧性。在浮浮沉沉数年之后,CTLA-4抑制剂又开始“复活”了。
时隔11年,CTLA-4抑制剂市场,终于又迎来了新鲜血液。2022年,阿斯利康CTLA-4抑制剂tremelimumab在美国获批上市,成为全球第二款获批上市的CTLA-4抑制剂。
3月21日,CTLA-4领域迎来了一笔久违的重磅交易。BioNTech以高达2亿美元的首付款,与昂科免疫就CTLA-4抑制剂ONC-392达成合作。
久违的新药问世、重磅交易,都透露出一个讯息,沉寂已久的CTLA-4抑制剂正在苏醒。那么,是什么使得一个已经被冷落多年的老靶点,老树发新芽?
/ 02 / 新机制、新技术的“救赎”
答案在于新技术、新机制的“救赎”。
CTLA-4抑制剂的机制颇为复杂,即便如今,科学家对CTLA-4抑制剂的机制也并未完全洞察清楚。
目前,针对CTLA-4抑制剂机制主要有两种不同的学说。
一种学说是“条件性激活派”。该学说强调,CD28可以激活T细胞,而CTLA-4会与CD28竞争并阻断T细胞激活,导致T细胞的活化受到抑制。CTLA-4抑制剂则可以通过阻断CTLA-4,从而重新激活T细胞分化、增殖为效应T细胞,以对抗肿瘤。
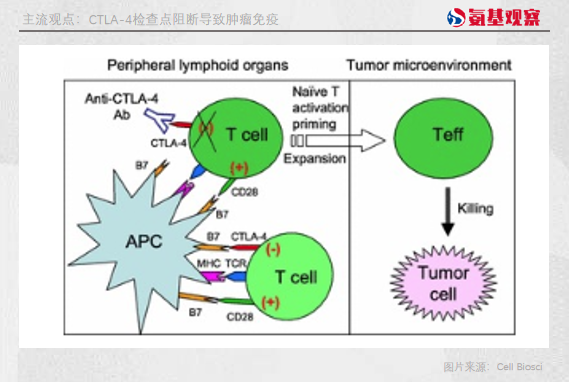
简单来说,CTLA-4抑制剂可以松开免疫系统的刹车,Y药的开发便是根据这一理论。
另一种学说是“Treg派”。该学说认为,CTLA-4抑制剂是通过抗体Fc受体介导的ADCC及ADCP效应,清除高表达CTLA-4的肿瘤局部Treg,解除Treg的免疫抑制效应,以达到对抗肿瘤的效果。
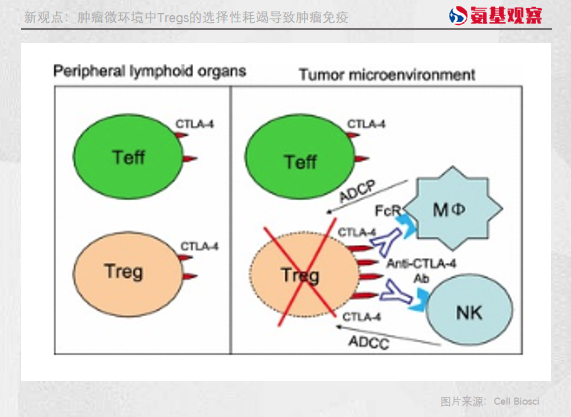
Treg细胞是一种抑制免疫功能的细胞,当T细胞与感染之间的战争结束后,Treg细胞就会发出攻击停止信号,从而抑制免疫效应。
在这一理论支撑下,新机制的CTLA-4抑制剂也处于研发中。比如,百时美施贵宝新开发的第二代CTLA-4抑制剂BMS-986218,便是在Y药的基础上进行改造,通过Fc修饰来增强ADCC功能消除Treg。
昂科免疫的ONC-392同样是“Treg派”代表,其是一个酸性敏感型CTLA-4抑制剂。在正常组织、器官境的PH下,其能够和CTLA-4发生强烈的相互作用。
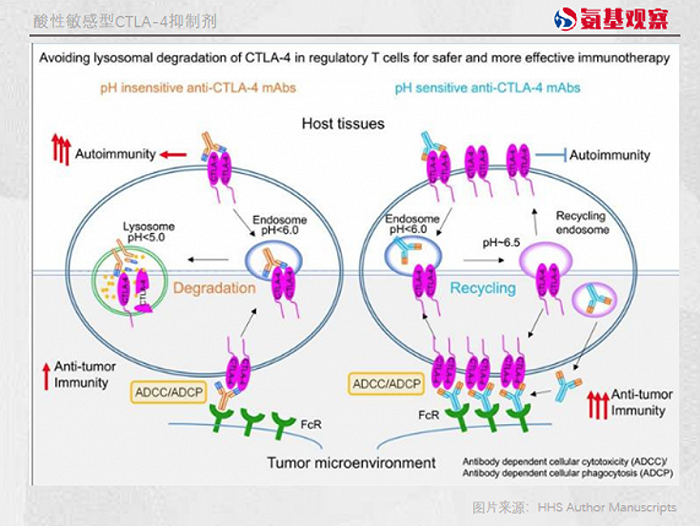
当PH值小于6,也就是处于肿瘤的酸性微环境中时,ONC-392则会迅速与CTLA-4分子分离,使CTLA-4避免被抗体诱导的溶酶体降解。通过这种方式,CTLA-4便不会被溶酶体降解,从而降低了CTLA-4抑制剂的毒性。
可以看到,通过新机制研发的CTLA-4抑制剂,正在试图突破CTLA-4的安全性桎梏。
除了新学说的出现,新技术的出现也在推动着CTLA-4抑制剂的发展。
比如百时美施贵宝研发的CTLA-4抑制剂BMS-986249。这一药物结合了CytomX公司的probody(前抗体)技术,在单抗上连接了一个掩蔽肽。改造后,BMS-986249在酸性环境下具有较强的结合活性,而在中性环境中其结合能力很大幅度降低。通过这种方式,BMS-986249得以有较好的安全性。
正是在新技术、新机制的双重推动下,此前遇冷的CTLA-4抑制剂,获得了新生的机会。
/ 03 / 向死而生的创新药
对于CTLA-4抑制剂来说,这一出“复活记”还未到终章。
如今CTLA-4抑制剂热度回升不假,但是在CTLA-4抑制剂作用机制尚未被彻底洞悉之前,无论是哪一条路,均存在着失败的风险。
这才符合创新药研发的规律。事实上,百时美施贵宝在2022年年报中,砍掉了处于临床2期的CTLA-4药物BMS986218。
大药企的一举一动向来是行业的风向标,尤其是在CTLA-4抑制剂领域,百时美施贵宝更是当之无愧的领头羊。如今领头羊放弃一款处于临床二期的CTLA-4抑制剂,背后蕴藏的风险不可忽略。
CTLA-4能否真正活过来,还需要更多的临床数据来给出答案。
但不管怎么说,CTLA-4已经重新站上舞台,药企们对于CTLA-4抑制剂的探索仍在继续。国内方面,天演药业、信达生物、和铂医药等均在研发第二代CTLA-4抑制剂。只要有人还在探索,CTLA-4重现昔日高光的机会,也就仍然存在。
复盘CTLA-4抑制剂的经历,你会发现,这并不令人陌生。创新药研发史上,最不缺的就是跌宕起伏的药物研发故事,在失败和成功的边缘上打转的靶点比比皆是。
起伏之中,总有人在坚守,投入精力、财力,持续进行药物的优化设计,验证靶点的可行性,这才有了药物的最终成功。
这个过程,充满了挫折、不确定性和质疑。有时候希望越大失望越大,有时候柳暗花明又一村。
然而,种种挑战与风险,不会改变人类健康和可持续性方面的持续需求。
创新药的发展,从来都是螺旋上升的;生物科技的前景,也从未如此光明。随着新技术、新机制的出现,那些曾经被否定的药物,也有可能重新焕发新的光芒。
只要那些敢于直面研发领域出现的各种问题,变挑战为机遇的奋斗者仍在坚持,那么希望就在。



评论