文|氨基观察 徐林卓
自身疾病领域,药王的迭代从未终止。
现任药王修美乐因为专利问题日薄西山,艾伯维管线中,另一款“药王”争夺者IL-23抑制剂瑞莎珠单抗则已经呼之欲出。
2022年销售额已达51亿美元,表现如日中天的瑞莎珠单抗,是艾伯维寄予厚望的下一款“药王”,是填补修美乐空缺的种子选手。
得益于机制优势,白细胞介素-23(IL-23)抑制剂在自身免疫疾病领域的天花板,超乎想象。
全球多款IL-23抑制剂,依靠银屑病适应症均取得了极为亮眼的表现。如今,IL-23抑制剂的适应症探索之旅还在继续,前景自然也会更加乐观。
不过,有人欢喜有人落寞。
对IL-23抑制剂领域虎视眈眈的巨头不在少数,但并非所有人都能脱颖而出,阿斯利康就成了落寞者。
6月1日,阿斯利康宣布退出IL-23抑制剂之争。原因不是有效性问题,也不是安全性缺陷,而是竞争格局原因。
这也预示着,IL-23抑制剂领域的淘汰赛已经开始。阿斯利康的退出,对于参与其中的国内药企来说,或许也要打起精神了。
01 “关键启动者”的狂想曲
IL23 是自身免疫疾病的“关键启动者”。
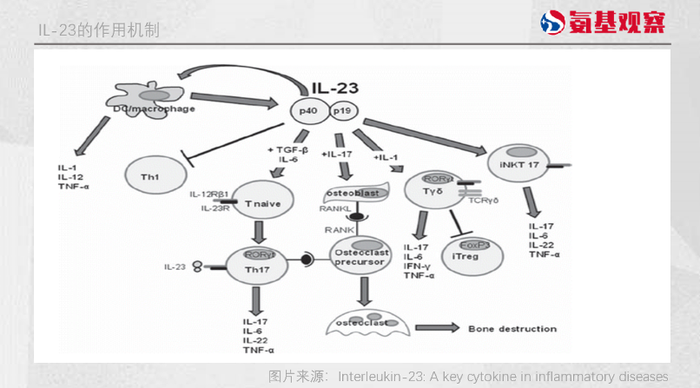
其主要由树突状细胞和巨噬细胞表达,在T细胞介导的免疫反应中处于更上游的位置,因此可能会造成严重的免疫级联放大效应。
例如,在银屑病发病机制中,当 IL23过度产生时会促进Th17细胞产生大量细胞因子,导致人体陷入“细胞因子增加——角质活化——活化的角质促进细胞因子增加”的无限循环。
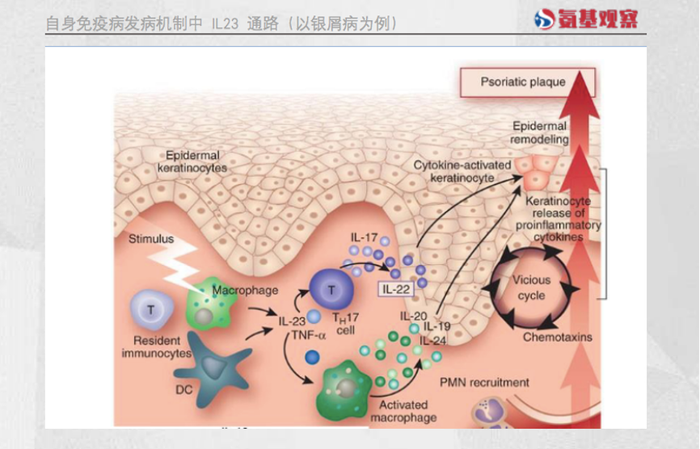
因此,阻断IL23是自身免疫病的重要治疗方法。在实际应用中,它也展现了极为突出的潜力。在银屑病领域,得益于上游机制的天赋,其相较于其下游的IL-17抑制剂,拥有效果更好、依从性更高的特点。
治疗效果方面,强生的古塞奇尤单抗力挫IL-17抑制剂领域的王者:诺华的司库奇尤单抗。
在头对头司库奇尤单抗的Ⅲ期临床试验中,48周后,古塞奇尤单抗组银屑病面积和严重程度指数减少90%患者比例(PASI 90反应)为84%(451/534),而司库奇尤单抗组达到PASI 90的患者比例为70%(360/514)。
依从性方面,使用IL-17抑制剂司库奇尤单抗的患者需要一年给药16次,而IL-23抑制剂古塞奇尤单抗一年只需给药6次。
效果更好、依从性更佳,使得IL-23抑制剂在不断蚕食IL-17抑制剂的市场。当然,IL-23抑制剂不会局限在银屑病领域,在克罗恩病等领域也展现了极为突出的想象空间。
IL-23主要在肠道中表达,对维护肠道稳态发挥重要作用,在过度表达时会造成肠道炎症。所以IL-23抑制剂对克罗恩病和溃疡性结肠炎也具有明显疗效。
总的来说,基于适应症广泛,给药间隔时间长,疗效更优,以古塞奇尤单抗为代表的IL-23抑制剂迅,在自身免疫疾病药物领域的地位逐步凸显。
02 海外药企的层层卡位
过去二十年,IL-23一直是海外大药厂的重要战场。
截至目前,全球已有5款IL-23抑制剂获批上市,其中最早上市的是强生的乌司奴单抗,于2008年获批。
当然,海外药企并没有陷入同质化竞争,而是不断将IL-23抑制剂的研发推向新的高度。
IL-23由p19亚基和p40亚基共同组成,其中p40亚基由IL23和IL12共享,因此靶向p40亚基的效果会更差。
强生的乌司奴单抗就是靶向IL-23的p40亚基,因为对IL-23的靶向定位作用不够精准,临床疗效逊于诺华的司库奇尤单抗。
在二者头对头临床试验中,治疗中重度银屑病患者52周后,司库奇尤单抗组PSAI 90的患者比例为73.3%,乌司奴单抗组达到PASI 90患者比例为59.8%。
之后,强生推出了二代抑制剂古塞奇尤单抗,靶向IL-23独有的p19亚基,属于IL-23p19单抗。
因为古塞奇尤单抗的临床疗效和用药间隔均优于司库奇尤单抗,二代抑制成为了IL-23抑制剂研发的主要方向,其余几款上市药物均为二代抑制剂。
尽管强生的古塞奇尤单抗是二代抑制剂的开创者,但成绩最好的却是艾伯维的瑞莎珠单抗(risankizumab)。
瑞莎珠单抗的临床疗效与古塞奇尤单抗相当,但一年只需用药4次,患者的依从性更高。
在艾伯维的推广下,瑞莎珠单抗的销售额迅速上涨,去年销售额为51.65亿美元,超过了司库奇尤单抗的47.88亿美元。而古塞奇尤单抗去年的销售额为26.68亿美元,仍有不少的差距。
面对二者的神仙打架,其他的IL-23抑制剂想要突破只能选择更换适应症。如,礼来的Mirikizumab便是以溃疡性结肠炎作为首个适应症获批上市的,对克罗恩病的研究也进入Ⅲ期临床试验阶段。
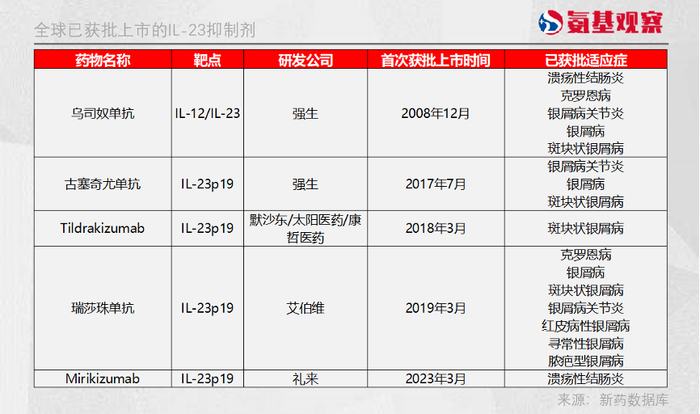
但强生和艾伯维也在迅速扩张该领域的适应症:
古塞奇尤单抗在克罗恩病和溃疡性结肠炎的研究均已进入Ⅲ期临床试验阶段;瑞莎珠单抗治疗克罗恩病适应症已在美国和欧盟获批,溃疡性结肠炎适应症已进入Ⅲ期临床试验阶段。
这让一些想要进入IL-23领域的药企选择了放弃。阿斯利康在今年6月公布,受竞争格局影响,将终止IL-23抑制剂brazikumab的开发计划,尽管其治疗炎症性肠病和克罗恩病均已进入Ⅲ期临床试验阶段。
03 国内药企慢了一截
与海外IL-23竞争已经进入白热化阶段不同,国内药企的发展相对较为缓慢。
目前,只有4家企业的IL-23抑制剂研发阶段超过临床。其中,康哲药业引进的IL-23抑制剂已经上市,康方生物、信达生物、石药集团均处于临床试验阶段。
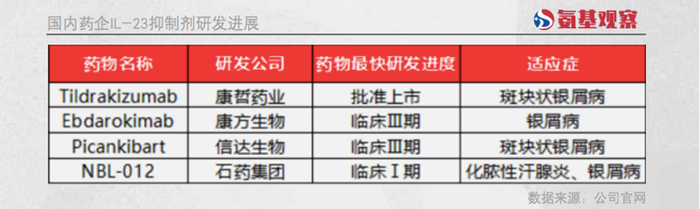
慢了一截的国内药企要想突围,必然会遭遇更多挑战。
首先就是海外药企的IL-23抑制剂已进军国内市场,依靠医保优势卡住身位。
强生的古塞奇尤单抗于2019年在国内获批上市,并且在今年进入了医保,价格降为4571元/支,北京地区患者报销后一年的使用费用为5485.2元,比上市价格节省了16万元!
而艾伯维的瑞莎珠单抗于7月6日申请在国内上市,如果后续也选择降价进入医保,也将是有力的竞争者。
其次,国内药企IL-23抑制剂的临床疗效也有待考验。
虽然康哲医药引进的Tildrakizumab于今年5月已在国内获批上市,但其临床疗效不及古塞奇尤单抗。
非头对头数据显示,治疗中重度斑块型银屑病患者12周,PASI 75患者的比例为63%;古塞奇尤单抗治疗中重度斑块型银屑病患者12周PASI 75患者比例为85%。
而康方生物的IL23抑制剂由于立项较早,跟随的是强生第一代抑制剂乌司奴单抗,靶向IL-23的p40亚基,因此后续竞争优势有待验证。
此外,海外药企已经开始升级药物的制剂形式。
强生最近公布了口服IL-23抑制剂JNJ-2113的Ⅱb期临床数据,各剂量组的治疗中度至重度斑块状银屑病的成年患者16周后,达到PASI 75/90/100的患者比例均高于安慰剂组;
每天接受100 mg JNJ-2113两次剂量组,达到PASI 75/90/100的患者比例最高,为78.6%、59.5%和40.5%。
临床数据优秀,并且以口服给药的形式极大提高了患者的依从性,与注射剂药物相比优势更明显。目前,JNJ-2113在国内也已经申请上市。
作为follow者的角色,国内药企在IL-23抑制剂领域的研发中,药物靶点、临床疗效、制剂形式上均处于落后的阶段,想要突破海外药企的统治,显然要加油了。



评论