文|公司研究室IPO组 王飞澍
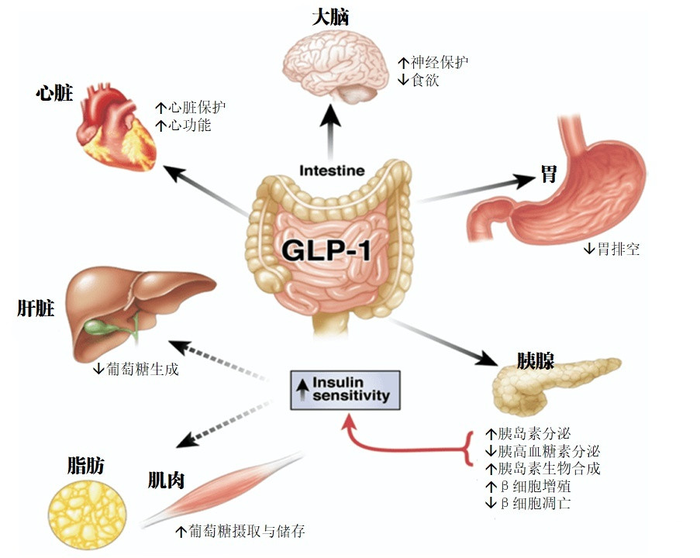
日前,广州银诺医药集团股份有限公司(简称“银诺医药”)公告称,已于2022年12月30日同中信证券签署上市辅导协议,正式启动IPO进程。据悉,银诺医药已拥有多项针对糖尿病、肥胖、非酒精性脂肪性肝炎等适应症的研发管线,其中,公司首个管线产品苏帕鲁肽已进入2型糖尿病适应症三期临床研究。这一产品上市后将成为我国首个自主知识产权的人源化长效GLP-1(胰高血糖素样肽-1)受体激动剂,也是资本方广泛看好的产品。
不过,银诺医药的GLP-1型产品虽为国内该领域的明星产品,但在全球范围内并不具备优势,国外医药巨头已有成熟产品上市,正在研发的苏帕鲁肽要想从巨头口中夺食,可能还面临着诸多不确定性因素。
01、先合作后独立,海归专家带来苏帕鲁肽
在糖尿病研究领域,加拿大多伦多大学下属机构班廷百思特研究所全球排名第一,在业内声名赫赫,银诺医药创始人王庆华正是是多伦多大学的终身教授及班廷百思特糖尿病研究所的常务委员。
在欧美市场,GLP-1药物早已成为最有前景的医药领域之一。GLP-1研究领域的奠基人和杰出领袖之一,加拿大多伦多大学的Daniel Drucker教授曾乐观预言:在不久的将来,GLP-1类药物将取代胰岛素成为糖尿病治疗的主线药物。亿欧智库在《2022年药品市场生命周期研究之GLP-1RA篇》预测,2022年到2030年,中国GLP-1RA市场规模将从56亿元增长至158亿,复合增速14%。
2014年,王庆华选择回国创业,彼时一级市场创新药投资还不是主流,根据当时的形势,王庆华选择了先跟昆药集团合作,银诺医药成为了昆药的控股子公司。直到2020年,银诺医药才开始了独立的市场化发展之路,旋即引来了投资者的关注。
天眼查显示,在启动IPO之前,银诺医药仅仅进行过两轮融资,最近的一轮是2021年底的A轮融资,优山资本、华创资本共同领投了1.2亿美元。
“当时的投资逻辑是产品驱动,GLP-1是糖尿病治疗中非常重要的角色之一,但中国糖尿病治疗有一个代际的差距。跟欧美国家相比,GLP-1在中国的普及率非常低,当时在中国的应用还不到5%。”曾参与了银诺医药A轮融资的华创资本投资人王冰洁表示,“银诺当时的GLP-1已经完成临床Ⅱa,在国内同类品种中银诺医药临床跑得最快,又做得非常扎实,当初我跟团队交流的印象也非常深刻。”
事实上,从目前的临床试验结果来看,银诺医药的苏帕鲁肽对糖尿病的治疗效果显著。一项随机、双盲、安慰剂对照、多剂量递增研究评估了苏帕鲁肽在T2D患者中的安全性、PK/PD和疗效,40名受试者以4:1的比例随机分配接受苏帕鲁肽(1,2,3和4mg)或安慰剂,其中4mg组接受1mg的适应性剂量以减少胃肠道反应。
PK结果显示,苏帕鲁肽的T1/2为∼207h,中位Tmax为60∼84h;PD结果显示,治疗7周后,苏帕鲁肽显著降低了空腹血糖,HbA1c降低1.3%并减轻体重。AE主要是轻度至中度胃肠道症状,没有一个受试者产生抗药物抗体,整体耐受性良好。
这还仅仅是在糖尿病方面的表现,苏帕鲁肽作为GLP-1类药物在减肥方面也有着良好的应用前景。
一个可以进行类比的是诺和诺德的司美格鲁肽注射液,据估算,该药物在正常情况下患者一年需要使用15支,人均年度治疗费用2700元,以此计算,GLP-1药物在肥胖患者中应用市场空间将达到243.6亿元。
王庆华曾不无自信地表示,苏帕鲁肽实现产业化后,将是一个实现10亿-30亿元工业产值和销售的重磅产品,将有可能改写中国生物制药产业的行业格局。
02、3期临床进行中,离产品上市尚远
苏帕鲁肽的前景虽然广阔,但距离上市销售还有一段距离。
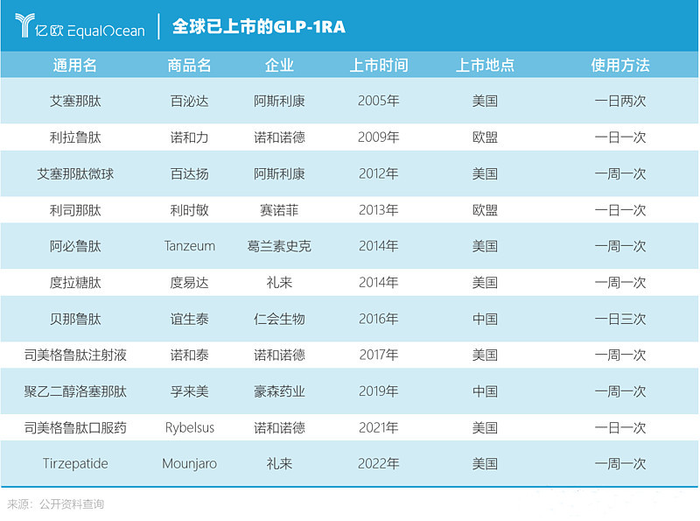
世界上首款GLP-1RA药物是2005年上市的艾塞那肽,这是一种短效药,一天需要注射两次,不过这仍然具有划时代的意义,此后,FDA接连批准了数种GLP-1RA,截至现在,全球已上市11种GLP-1RA。
全球GLP-1药物的市场格局,先后被利拉鲁肽、度拉糖肽和司美格鲁肽主导,尤其是后两者,2021年,司美格鲁肽注射液和口服药的总销售额已经达到约61亿美金,度拉糖肽则约为65亿美金。业内乐观预计,司美格鲁肽将有望在接下来大幅改变GLP-1RA的市场格局。
因此,尽快完成苏帕鲁肽的研发并上市销售,就成了银诺医药能否在巨头竞争格局中分得一杯羹的关键。对此,在2020年初时,王庆华曾表示:“我们现阶段需要做的是用最短的时间在国内完成CFDA规范的苏帕鲁肽临床研究,然后尽可能快地把创新药推向市场,期望在2020年或者2021年上市。”
但事实却是,时间已经来到了2023年,而银诺医药的上市时间仍未有明确时间表。最新消息显示,2022年7月下旬,苏帕鲁肽“在10个月内完成两项3期临床千余例患者入组计划”,而早在2021年底,该药就已经进入了3期临床研究,根据新药研发流程,新药3期临床研究时间可能长达1年或以上。
即便完成了3期临床,苏帕鲁肽离上市还将有一段距离。一般而言,新药物经过3期临床研究证明药物安全性和有效性之后,才可以向(C)FDA提交上市申请,而近五年,中国药监局的中位审批时长为400-450天。
也就是说,就算一切顺利,苏帕鲁肽至少也需要一年多才能上市,而这在火热的GLP-1药物市场中,却意味着许多变数。
03、进口药占据超90%市场份额,仿制药也在磨刀霍霍
就市场竞争格局而言,银诺医药面临的形势比较严峻,很可能遭遇国际巨头与国内仿制药的夹击。
首当其冲的就是国际巨头统治级的优势。目前,诺和诺德在中国的GLP-1RA市场占据绝对统治地位,中国GLP-1RA市场份额的超90%都被7款进口药所占据。而且,在注射液的基础上,国外医药巨头已经开始着力开发更方便使用的口服型GLP-1类药物。
2019年,诺和诺德的口服司美格鲁肽首先研发成功,目前,其正在研发新一代口服GLP-1RA,该药将有望剂量大幅缩减且半衰期更长。此外,礼来与罗氏旗下的日本中外制药株式会社达成协议,开发口服GLP-1RAOWL833,同时,后者自己也在开发艾塞那肽的口服制剂ORMD-0901。
同一赛道的江苏豪森药业推出的聚乙二醇洛塞那肽,是中国首个自主创新长效GLP-1类降糖药物,也是全球第一款PEG化的长效降糖药物,它的使用频次是一周一次。2020年进入医保后,日治疗费用只需自付8元。2020年,其营收增速达764.44%,2021上半年则达到了622.74%。
此外,国内还有不少医药企业也正在布局GLP-1。除已上市的8款GLP-1 受体激动剂外,Tirzepatide礼来已申报NDA;除苏帕鲁肽之外,还有 6 款药物处于临床 III 期,包括IBI362 (信达生物)、格鲁塔株单抗(鸿运华宁)、聚乙二醇化艾塞那肽(派格生物)、艾本那肽(常 山生化)、Efpeglenatide (韩美药品)等。GX-G6(石药集团),ecnoglutide(先为 达生物),HR170331(恒瑞医药),TTP273(中美华东)等药物处于临床 II期。
这还只是原研药的研发,如果再算上仿制药,那么形势将更为紧迫。通常而言,仿制药的研发费用仅为数十万美元,与原创药动辄数以亿计的研发费用相比,成本优势尤为显著,且研发周期也更短。
由于利拉鲁肽和艾塞那肽微球在中国的专利已到期,鉴于此前的销售佳绩,国内仿制药企纷纷开始发力,GLP-1市场将很快迎来一大波竞争对手。目前,国内至少有11家企业仿制利拉鲁肽,6家企业仿制艾塞那肽及艾塞那肽微球。其中,华东医药为国内首家利拉鲁肽报产的企业,通化东宝预计2022年上半年报产,为国内第二家。
因此,在国际医药巨头、国内竞争对手以及仿制药企等的竞争之下,已经比原计划推迟上市且并没有特殊优势的银诺医药,压力不可谓不大。



评论